钢结构的腐蚀与涂装防护原理
发布时间:2018-09-13
钢结构是金属中的一个大类,为了提高钢结构的使用寿命,必须在了解金属的腐蚀机理的基础上,来控制钢铁的腐蚀速度,探求防护的最佳办法。
金属腐蚀的基本原理
当金属与周围介质发生化学反应或电化学反应后,就会形成金属的化合物, 使金属失去原有的光泽、强度、韧性等,金属就受到了破坏,这就是金属的腐蚀。金属的腐蚀有两个基本类型。
化学腐蚀过程
化学腐蚀是气体或液体介质与金属表面发生化学作用,产生化合物,从而使金属表面遭受腐蚀损坏的过程。如对钢铁进行热轧、焊接、铆接、切割等高温加热,钢铁和空气中的氧反应,在钢铁表面形成黑色氧化皮;又如含硫石油等有机物质作用于金属时所发生的腐蚀;在干燥气体介质中发生的腐蚀等等;这些都是化学腐蚀的过程。化学腐蚀的特点是腐蚀产物直接生成在发生反应的金属表面,生成物的厚度和疏松紧密程度决定了金属腐蚀的速度。化学腐蚀是一种没有电流产生的腐蚀过程。
电化学腐蚀过程
金属在大气中的锈蚀主要是电化学腐蚀。金属的电化学腐蚀是自偶电池发生的。即当电解液中有任何两种电极电位不同的金属成为阳极而被腐蚀。因此,电化学腐蚀的进行必须具备这样3个基本条件:一是有不同的金属存在;二是不同的金属处于相接触之中;三是不同金属同时存在于电解质溶液中。另外钢铁表面具有由于杂质、氧化皮的缺陷、晶体结构、机械或热加工等原因产生的不均匀性。从环境方面讲,则有温度差、氧浓度的不均匀性,特别是在大气腐蚀的条件下, 钢铁表面吸附一层水膜而形成许多微小的原电池,这些都是造成发生电化学腐蚀的条件。钢铁表面的电化学腐蚀原理详见下图。
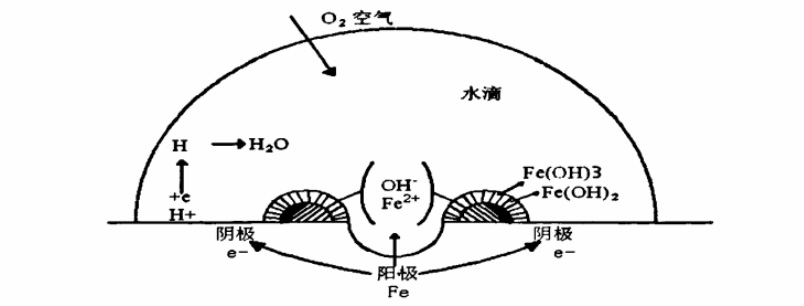
产生这种腐蚀的条件是水和氧气共同存在。铁原子比较活拨,易失去电子,和水释放的氢氧根OH-相结合生成氢氧化亚铁,它溶于水。其反应方程式如下:
Fe2++20H-=Fe(OH)2
水中的氢氧化亚铁和氧结合生成铁锈即氢氧化铁,其反应方程式如下:
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
总之,电化学腐蚀的基本过程是由阳极发生氧化反应、电子流动、离子迁移和阴极还原反应这四个环节组成,缺少任何一个环节都不可能发生电化学腐蚀
上一条:
氟碳金属漆施工工艺
下一条:
镀锌板用漆应该如何选择
![]()
![]()
![]()
![]()